Залози внутрішньої секреції, або ендокринні, є особливою системою органів, що виділяють біологічно активні речовини — гормони. До ендокринних залоз належать: гіпофіз, передній гіпоталамус, епіфіз, щитовидна і паращитовидні, підгрудинна, надниркові, острівцевий апарат підшлункової залози, статеві.
Ендокринні залози мають великий вплив на обмін речовин, на фізичний і психічний розвиток організму дитини. В дитячому віці значення ендокринних залоз особливо велике, оскільки вони беруть участь в регуляції таких важливих для організму процесів, як ріст і розвиток (диференціювання). Тому при розладах функцій залоз внутрішньої секреції у дітей виникає своєрідна клінічна картина, яка не зустрічається у дорослих. Одна й та ж аномалія залоз, яка у дорослих викликає оборотні зміни, у дитячому віці може призвести до формування невиліковного психічного і фізичного дефекту.
Крім того, усі види обміну речовин — водний, мінеральний, вуглеводний, білковий і жировий — відбуваються за участю гормонів. Порушення діяльності ендокринних залоз призводить нерідко до різких змін в обміні речовин, що в свою чергу є причиною серйозних захворювань у дітей.
Розглянемо особливості функціонування ендокринних залоз в дитячому віці.
Щитовидна залоза — одна з найактивніших залоз внутрішньої секреції, гормональна функція якої значною мірою визначає інтенсивність обміну речовин, а в структурі ендокринної патології дитячого віку захворювання Щитовидної залози посідають одне з основних місць. Особливо це актуально Для зон, забруднених радіонуклідами.
Про важливе функціональне значення щитовидної залози для розвитку Дитини свідчить перш за все рання її закладка у ембріона. Вже в кінці 3-4-го тижня ембріонального періоду щитовидна залоза закладається у вигляді великого валика з вентральної стінки глоткового відділу кишечника. У Подальшому щитовидна залоза дуже швидко розвивається і вже до 4-го місяця внутріщньоутробного життя має цілком сформовану структуру. Вже в цьому періоді вона складається з двох часточок і перешийка.
До кінця 2-го місяця внутрішньоутробного розвитку щитовидна залоза функціонально неактивна, оскільки ще не має фолікулярної структури, характерної для зрілого життя. Але починаючи з кінця 2-го місяця внутрішньоутробного розвитку, з’являються фолікули, і в їх порожнинах накопичується тиреоглобулін, який спочатку не містить йоду і не бере участі в синтезі тиреоїдних гормонів. Через декілька днів тиреоглобулін здатний захоплювати неорганічний йод, що надходить з кров’ю від матері. В кінці 3-го місяця внутрішньоутробного розвитку починається синтез тироксину і трийодтироніну. Але спочатку в крові вони циркулюють у зв’язаному стані не з тироксинзв’язуючим глобуліном, а з альбумінами, оскільки синтез тироксинзв’язуючого глобуліну відсутній. Він спостерігається з кінця 5-го місяця внутрішньоутробного розвитку і відмічається його інтенсивне зв’язування з тироксином.
У крові сліди тироксину виявляються з кінця 3-го місяця внутрішньоутробного періоду, а потім концентрація його швидко підвищується, становлячи до кінця 6-го місяця 50% величини концентрації у крові дорослої людини — відповідно 26±3 нг/мл і 69± 1,3 нг/мл, а на 8-9-му місяці перевищує в 1,5 раза цифри у дорослого — 99±11) нг/мл.
Підтвердженням високої концентрації тироксину і високої функціональної активності щитовидної залози може бути факт покращення загального стану і зменшення вираженості симптомів гіпотиреозу у вагітних, у яких знижена функція щитовидної залози.
Крім екскреції тироксину і трийодтироніну, в стінці фолікулів щитовидної залози, а також парафолікулярно зустрічаються С-клітини, що виробляють гормон — кальцитонін, який знижує рівень кальцію в крові. Під його впливом гальмується резорбція оксіапатиту кісток і підсилюється його відкладання в органічному матриксі кісткової тканини. Тому кальцитонін має важливе значення в процесах регуляції остеогенезу і скелетоутворення. Кальцитонін є антагоністом паратгормону. Кальцитонінпродукуючі клітини виявляються в щитовидній залозі на 14-му тижні внутрішньоутробного розвитку, і в цей час визначається продукуючий кальцитонін.
Під час пологів після відокремлення дитини від матері відмічається високий вміст кальцитоніну в крові. Це розцінюється як його участь в родовому стресі. Висока концентрація кальцитоніну сприяє зниженню рівня кальцію в крові, що обмежує надмірну активацію ряду ендокринних залоз, для яких іон кальцію служить стимулятором секреції. До таких залоз належать гіпофіз, кора наднирників, P-клітини апарату підшлункової залози.
При народженні щитовидна залоза у дитини відносно більша, ніж в наступні роки життя. Протягом першого року життя вираженого росту паренхіми щитовидної залози не відбувається, але потім починається бурхливе збільшення маси залози до 5-6-річного віку. У подальшому темп росту уповільнюється аж до передпубертатного періоду. Але у віці 12-15 років відмічається особливо бурхливий ріст щитовидної залози, причому вона настільки збільшується в розмірах, що можна відмітити деяку припухлість залози і це викликає турботу у батьків. В нормі залоза не пальпується і не помітна при зовнішньому огляді. Важливо підкреслити, що розміри щитовидної залози суттєво залежать від кровонаповнення.
Збільшення розмірів залози корелює з підсиленням її функціональної активності, яке спостерігається у віці від 6 міс до 2 років. Найбільш виражена активність щитовидної залози спостерігається в передпубертатному періоді (у хлопчиків — в 10-12 років, у дівчаток — дещо раніше) і досягає максимального рівня у представників обох статей у віці 14-15 років.
Гістологічна структура щитовидної залози в період новонародженості вказує на незавершеність її будови: фолікули ще погано виражені і в їх просвіті немає або майже немає колоїду; епітелій фолікулів циліндричний; мають місце скупчення епітеліальних клітин, які розділені ніжними сполучнотканинними прошарками.
З віком в залозі збільшується кількість фолікулів і вміст колоїду, зникає циліндричний епітелій і з’являється плоский. Остаточна гістологічна структура залози завершується після 15 років.
Основними гормонами щитовидної залози є тироксин, трийодтиронін і тиреокальцитонін. Гормони щитовидної залози, як відмічалося раніше, значно впливають на обмінні процеси. Зокрема, показано, що гормони щитовидної залози підсилюють газообмін і перш за все — поглинання кисню тканинами і виділення вуглекислого газу, впливають на білковий обмін, посилюючи як асимілятивні, так і дисимілятивні процеси. Крім того, гормони щитовидної залози значно впливають на процеси обміну жирів і вуглеводів, посилюють виділення води і беруть участь в обміні хлоридів, впливаючи на мінеральний обмін і розвиненість скелета, а також визначають обмін калію і кальцію в організмі.
Таким чином, ці гормони є універсальними стимуляторами метаболізму, росту і розвитку. Природно, що недостатня або надмірна продукція гормонів щитовидної залози викликає різноманітні і значні порушення життєдіяльності Дитячого організму.
В клінічній практиці може спостерігатися як підвищення (гіперфункція), так і зниження (гіпофункція) активності щитовидної залози, які мають ряд специфічних клінічних ознак.
Паращитовидні залози з’являються на ранніх стадіях ембріонального Розвитку. їх можна виявити у ембріона на 6-му тижні внутрішньоутробного розвитку. У цей період починається секреція паратгормону. Концентрація Ц^ратгормону в крові пупкових судин близька до такої в крові матері (0,07- ’ з нг/мл), але підтримуються ці концентрації незалежно.
Паращитовидні залози функціонують найбільш активно до 4-7 років. Клітинний склад залоз представлений в основному світлими головними клітинами, які дуже активно синтезують і секретують паратгормон. Після 6-7- річного віку появляються більш темні оксифільні клітини, які розцінюють як ознаку інволюції головних клітин. Концентрація паратгормону в крові в цей час становить в середньому 0,3-0,8 нг/мл.
Кількість оксифільних клітин до 10 років значно збільшується. До 12 років в паренхімі залози з’являється жирова тканина, яку розглядають як подальший прояв інволюції цих залоз.
Фізіологічне значення паратгормону полягає в тому, що він стимулює реабсорбцію кальцію в дистальних канальцях нирок, інгібує реабсорбцію фосфату в проксимальних і дистальних канальцях нирок, викликаючи фосфатурію і знижуючи концентрацію фосфору в крові. Крім того, паратгормон стимулює процес гідроксилювання неактивного вітаміну D в його активний метаболіт D3 (1,25-дигідроксикальциферол), що призводить до підсилення всмоктування кальцію в кишечнику. Паратгормон стимулює кількість остеокластів, а потім сприяє збільшенню кількості остеобластів, які є кісткоутворюючими клітинами.
Механізм дії паратгормону на організм обумовлює клінічну симптоматику, яка спостерігається при гіпер- або гіпофункції паращитовидних залоз.
Гіпофіз в системі ендокринних залоз посідає особливе місце і його називають головною ендокринною залозою, оскільки він виробляє тропні гормони, які мають стимулюючий вплив на інші залози внутрішньої секреції.
Гіпофіз розташований в так званому турецькому сідлі, що представляє собою кісткове заглиблення у підвалині черепа. Тонкою ніжкою гіпофіз зв’язаний з гіпоталамусом.
Гіпофіз закладається на 4-му тижні внутрішньоутробного життя з двох окремих зачатків: ектодермального епітелію, з якого формуються передня (аденогіпофіз) і середня частки, а з другого зачатка — виросту проміжного мозку — утворюється задня частка (нейрогіпофіз).
Починає функціонувати гіпофіз дуже рано, і на 9-10-му тижні внутрішньоутробного життя виявляється синтез адренокортикотропного гормону (АКТГ; рис. 46).
Передня частка гіпофізу, що становить 75% усієї маси залози, складається з еозинофільних, базофільних і хромофобних клітин. У новонароджених в передній частці переважають базофільні гранулоцити, які дуже часто дегранульовані, що вказує на їх високу функціональну активність. Клітини передньої частки гіпофізу виробляють і виділяють в кров шість гормонів: АКТГ, соматотропний (СТГ), тиреотропний (ТТГ) і три гонадотропних — фолікулостимулюючий, лютеїнизуючий, лактогеннийі Виділення СТҐ пов’язують з функцією еозинофільних, а гонадотропних гормонів базофільних клітин.
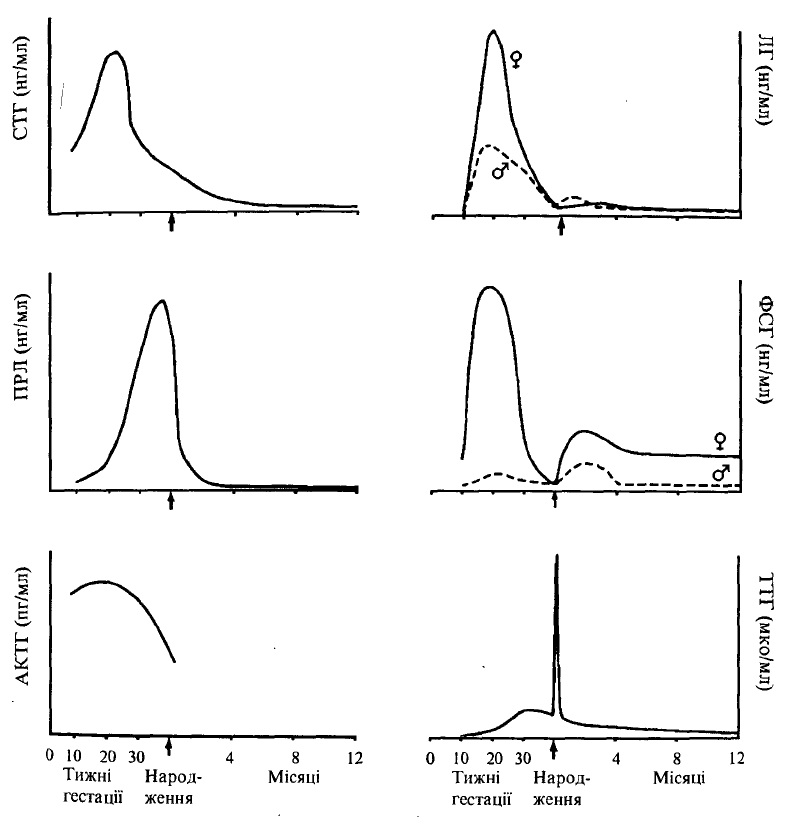
Рис. 46. Динаміка секреції гормонів гіпофіза під час гестації та в ранній постнатальний період.
СТГ – соматотропний гормон; ПРЛ – пролактин; АКТГ – адренокортикотропний гормон г – лютеїнизуючий гормон; ФСГ – фолікулостимулюючий гормон; ТТГ – тиреотропний гормон;
В середній частці виробляється меланоформний (або меланоцито-отимулюючий) гормон і вона становить лише 1-2% усієї маси залози.
Задня частка гіпофізу становить близько 18-23% усієї маси залози і виділяє та гормони: окситоцин і вазопресин (антидіуретичний гормон — АДГ), які продукуються нервовими клітинами, ядрами гіпоталамусу і у вигляді нейросекрету транспортуються в задню частку гіпофіза.
Гіпофіз виявляє енергійний ріст протягом перших чотирьох років життя і особливо в період статевого дозрівання.
Різноманітність синтезуючих гормонів і їх функціональної активності обумовлює поліморфність клінічної картини захворювань, які розвиваються внаслідок порушення функцій різних часток гіпофізу.
Епіфіз (шишковидна залоза) закладається на 6-7-му тижні внутрішньоутробного розвитку як випинання покривної пластинки проміжного мозку. Секреція гормонів починається на 3-му місяці внутрішньоутробного розвитку.
Епіфіз виробляє гормон мелатонін, фізіологічна дія якого полягає в тому, що він пригнічує секрецію гонадотропінів аденогіпофізом, викликає затримку статевого розвитку, впливає на пігментний обмін і пігментні тканини шкіри.
Відмічені вікові особливості функціонування епіфізу. Своєї максимальної активності він досягає до 5-7 років. Саме цей факт, очевидно, пояснює те, що ще до цього віку відсутні вторинні статеві ознаки, і повільно формуються статеві відмінності.
Після 10 років епіфіз підлягає зворотному розвитку. До початку статевого дозрівання відбувається різке зниження рівня мелатоніну в сироватці крові, що, можливо, і становить складову частину сигналу, який «запускає» пубертатний період.
Підвищення функції епіфізу призводить до зниження статевої функції і затримки статевого розвитку, тоді як гіпофункція супроводжується передчасним статевим дозріванням.
Підшлункова залоза належить до залоз з подвійною секрецією: зовнішньою (екзокринною) і внутрішньою (ендокринною). Як залоза внутрішньої секреції вона належить до системи травних залоз, і панкреатичний сік, який вона виробляє, містить більш ніж 20 ферментів (гастрин, секретин, холецистокінін та ін.).
Морфологічним субстратом ендокринної функції підшлункової залози служать острівці Лангерганса, який описав їх в 1869 р. Кількість острівців по відношенню до усієї тканини залози становить у дорослої людини 1-3%. У новонароджених і дітей раннього віку ендокринна частина підшлункової залози розвинена краше, ніж екзокринна.
Підшлункова залоза закладається на 4-му тижні внутрішньоутробного життя з ентодермального листка, але сильний розвиток залози починається з 6,5 міс. Остаточного розвитку підшлункова залоза досягає до 25 років.
Гормони підшлункової залози починають продукуватися неодночасно. З кінця 2-го місяця внутрішньоутробного життя a-клітини починають виділяти глюкагон, а до кінця 3-го місяця в (3-клітинах виявляється інсулін, а пізніше в D-клітинах появляється третій з основних гормонів підшлункової залози соматостатин.
Вказані гормони мають виражену біологічну дію, і в даний час відомо більше ЗО різних ефектів, які вони викликають.
Процес розвитку підшлункової залози продовжується і після народження дитини. При цьому спостерігається процес утворення нових острівців. Протягом першого року життя кількість тканини підвищується за рахунок збільшення кількості острівців. У старшому віці острівцева тканина продовжує збільшуватися за рахунок гіпертрофії.
У новонародженого кількість острівцевої тканини (ендокринної) переважає над ацинозною (екзокринною). В період народження маса острівцевої тканини становить 6% маси усієї залози, а в кінці року — менше 1% (як у дорослих).
У клітинних популяціях підшлункової залози у дитини (3-клітини переважають над a-клітинами. Причому кількість (3-клітин у дитини після народження збільшується з 50 до 70% до 6 міс. Кількість a-клітин при цьому залишається стабільною (20%), а число клітин, що секретують соматостатин, зменшується з 30 до 15%.
Таке співвідношення тканин вказує на перевагу синтезу інсуліну над утворенням глюкагону. В дитячому віці концентрація інсуліну хвильоподібно змінюється. Рівень інсуліну підвищується в період інтенсивного росту, забезпечуючи високу швидкість анаболічних процесів.
Із захворювань підшлункової залози, що супроводжуються порушенням функції її ендокринної частини, найважливіше клінічне значення має цукровий діабет.
Наднирники закладаються рано в ембріогенезі. При народженні функція кори наднирників висока, і на 2-му тижні життя дитини з розрахунку на одиницю поверхні тіла утворююча кількість кортикостероїдів така ж, як і у дорослих. При народженні відсутній добовий ритм секреції кортикостероїдів. Концентрація їх у новонародженого коливається незначно протягом доби. Добовий ритм секреції кортикостероїдів формується на 3-му тижня життя: рівень кортизолу найбільш високий вранці і знижується ввечері. На встановлення ритму впливає режим харчування дитини.
У новонароджених, на відміну від дорослих, переважає синтез 17- дезоксикортикостероїдів над 17-оксикортикостероїдами. Це має певне біологічне значення, оскільки 17-дезоксикортикостероїди виявляють менший катаболічний вплив, а отже, і менше перешкоджають росту, ніж 17- оксикортикостероїди.
Для мозкової речовини наднирників характерне пізнє формування і Повільний розвиток в онтогенезі. Синтез норадреналіну в ньому починається Наприкінці 3-го — початку 4-го місяця внутрішньоутробного періоду.
Адреналіну у плода утворюється мало.
У новонародженого мозкова речовина розвинена відносно слабко.
Кількість хромафінних клітин збільшується в основному після народження, особливо з 3-4 до 7-8 років. Тільки до 10 років мозкова речовина за своєю масою переважає кіркову.
Незважаючи на це, активність симпатоадреналової системи проявляється відразу після народження. З перших днів новонароджений здатний реагувати на стресові подразники підвищенням секреції катехоламінів, в основному норадреналіну (на відміну від дорослих). Однак мозкова речовина наднирників новонародженого реагує на стрес менш активно, ніж у дорослого. Знижена реакція його компенсується значним активуванням параганліїв симпатичної нервової системи, що виробляють катехоламіни.
У віці від 1 до 3 років секреція катехоламінів набуває добової і сезонної циклічності. Екскреція адреналіну мінімальна вночі і значно посилюється у весняний період.
Отже, найважливіші особливості ендокринної системи в дитячому віці такі.
- У кожному віковому періоді має місце функціональне переважання тієї чи іншої ендокринної залози і спостерігається гетерохронія їх розвитку та інволюції:
а) в періоди внутрішньоутробного розвитку і новонародженості найбільш активна щитовидна залоза і симпатоадреналова система;
б) в грудному віці виражений інкреторний вплив щитовидної і загрудинної залоз;,
в) в період молочних зубів високу активність має гіпофіз і задгрудинна залоза;
г) в передпубертатному періоді зростає значення інкрету статевих залоз, щитовидної залози і гіпофізу;
д) в пубертатному віці переважає активність статевих залоз і чітко виявляється дія наднирників.
- Порушення функціональної активності ендокринного апарату у дітей спостерігається частіше, ніж у дорослих. Це пояснюється незавершеністю будови ендокринних залоз, лабільністю регуляторних механізмів.
- Між усіма ендокринними залозами існує інтимний корелятивний зв’язок, але тільки до 6-7 років виникає чітка синхронна їх взаємодія.
- У ростучому організмі взаємовідношення між ендокринними залозами відрізняються великою рухливістю, а функціональні резерви гормонів відносно не великі. Тому різноманітна дія на організм може викликати у дітей суттєві порушення ендокринної регуляції розвитку.
- Для дітей характерні полігландулярні розлади ендокринної системи.